 文:藍萍|圖:編輯部
文:藍萍|圖:編輯部
特發性肺纖維化 (Idiopathic Pulmonary Fibrosis,IPF) 是一種致命的間質性肺病,可治選擇很稀少,預後也很差,往往需要靠心肺移植才能存活。臺大醫院醫療團隊今(25)日公布研究成果,發現內質網蛋白(TXNDC5)在肺臟纖維化疾病進展關鍵角色,倘若能發展藥物給予抑制,患者可望獲得治療,甚至可用在武漢肺炎引起肺纖維化。
臺大醫院內科副教授暨主治醫師楊鎧鍵研究團隊發現內質網蛋白thioredoxin domain containing 5 (TXNDC5)在肺臟纖維化形成中扮演重要角色,該論文於2020年8月26日刊登於頂尖期刊「自然通訊」(Nature Communications)。
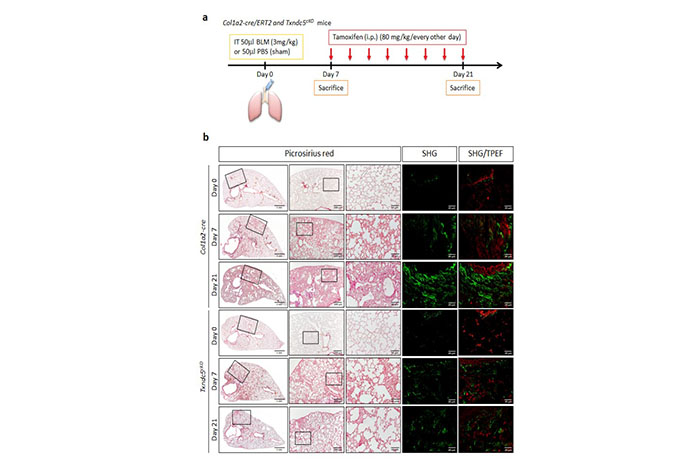
楊鎧鍵表示,依照評估,臺灣大約有5千多名特發性纖維患者,目前病因不明,臨床上可用於治療患者的藥物選擇稀少,治療效果不明確,預後也很差,患者從診斷自死亡平均只有2至5年時間,是所有肺纖維化中最嚴重的一種。
楊鎧鍵說明,研究團隊發現內質網蛋白TXNDC5是一種蛋白質雙硫異構酶,主要位於細胞的內質網,被認為和催化蛋白摺疊以及參與胞內氧化還原反應有關。在2018年研究發現TXNDC5在心臟纖維化中扮演重要角色。由博士班學生李姿涵延續在心臟的研究,更進一步發現TXNDC5會造成肺臟纖維母細胞的大量活化增生及胞外基質堆積,引起肺臟纖維化。
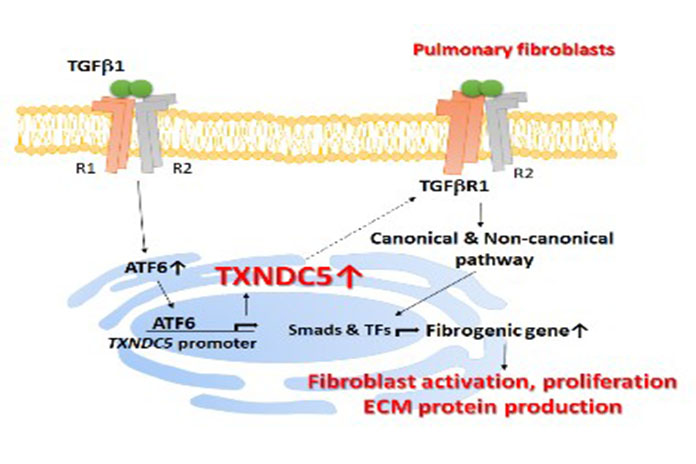
李姿涵提到,在IPF病患肺組織以及肺臟纖維母細胞中發現TXNDC5基因及蛋白表達量比正常人高,而在小鼠的肺臟纖維化動物模型中也證實,利用誘導型CRISPR/Cas9基因編輯技術敲除纖維母細胞中TXNDC5基因表現,能有效減緩肺臟纖維化之進程並改善肺功能。
楊鎧鍵指出,器官纖維化是組織受損後的修復反應,但持續而過度的纖維化卻也是造成器官功能喪失,甚至走向衰竭的重要原因,目前針對器官纖維化缺乏專一而有效的治療藥物,未來希望能將實驗室開發抑制TXNDC5的藥物應用在心臟及肺臟纖維化的患者,也將著手探討應用在其他組織纖維化,如腎臟及肝臟纖維化相關疾病的可能性,希望也能為慢性腎病變及肝硬化患者的治療帶來新的曙光。







